Jakarta -
Dalam pernyataan resminya Badan Pengawas Obat dan Makanan (BPOM) RI telah meminta industri untuk berhenti mendistribusikan obat hipertensi mengandung valsartan produksi Zhejiang Huahai Pharmaceuticals, Linhai, China. Hal tersebut bermula dari temuan zat pengotor Nitrosodimethylamine (NDMA) oleh Badan Pengawas Obat Eropa (EMA) pada awal Juli lalu.
Menurut Reuters sejak itu Zhejiang Huahai meminta distributor dan konsumen mengembalikan produk-produknya.
Disebutkan oleh BPOM bahwa di Indonesia produk ditarik sukarela oleh produsen. Beberapa obat yang ditarik meliputi Varten Tablet 80 mg dan 160 mg buatan PT Actavis Indonesia serta Valesco Kaplet Salut Selaput 40 mg, 80 mg dan 160 mg buatan PT Dipa Pharmalab Intersains.
ADVERTISEMENT
SCROLL TO CONTINUE WITH CONTENT
Sebenernya apa sih obat valsartan itu? Yuk simak fakta-fakta yang dirangkum detikHealth berikut:
Melebarkan pembuluh darah
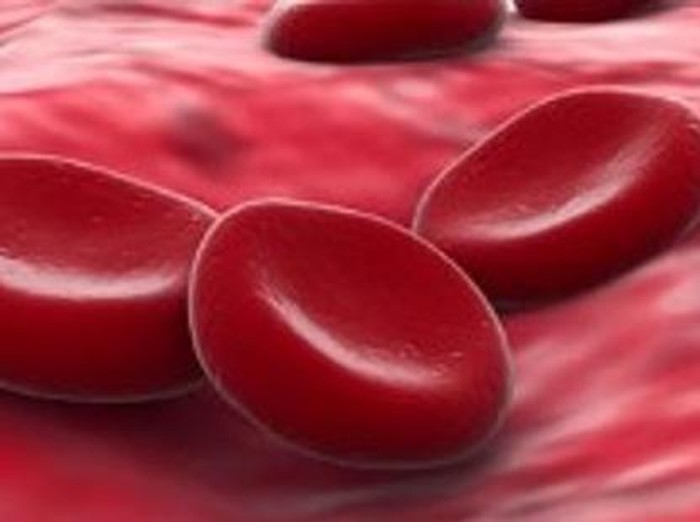 Foto: thinkstock
Foto: thinkstock
|
Menurut keterangan BPOM valsartan adalah obat oral yang masuk dalam kategori antagonis reseptor angiotensin II. Obat dalam kategori tersebut bekerja dengan cara menghambat reseptor angiotensin yang dapat berujung pada pelebaran pembuluh darah.Ketika pembuluh darah melebar maka tekanan darah akan berkurang.
Untuk hipertensi dan gagal jantung
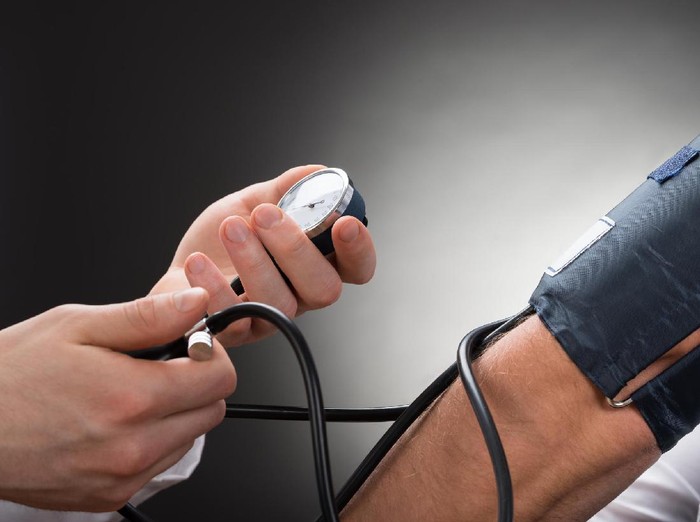 Foto: Thinkstock
Foto: Thinkstock
|
Karena sifatnya yang dapat melebarkan pembuluh darah valsartan sering dipakai untuk mengobati hipertensi dan gagal jantung. Kadang valsartan juga dipakai pada kasus serangan jantung untuk mengurangi risiko kematian dan waktu perawatan di rumah sakit.
Ditemukan perusahaan Swiss
 Foto: Rahma Lillahi Sativa
Foto: Rahma Lillahi Sativa
|
Valsartan awalnya dikembangkan oleh perusahaan farmasi Norvatis asal Swiss dengan nama Diovan. Tapi setelah patennya habis di tahun 2012 banyak perusahaan menggunakannya untuk membuat obat generik termasuk oleh Zhejiang Huahai.
Ditarik karena risiko kanker
 Foto: Thinkstock
Foto: Thinkstock
|
Obat mengandung valsartan yang diproduksi Zhejiang Huahai ditarik karena ditemukannya zat pengotor NDMA. Menurut ahli kemungkinan ini terjadi ketika perusahaan mengubah proses produksinya di tahun 2012.NDMA dalam beberapa studi disebut berhubungan dengan risiko kanker. Para ahli di Badan Pengawas Obat Eropa mengaku masih mengukur dampak pada pasien akibat konsumsi obat valsartan yang terkontaminasi ini.
Banyak disuplai perusahaan China
 Foto: Thinkstock
Foto: Thinkstock
|
Menurut Reuters saat ini kebutuhan obat valsartan di seluruh dunia banyak disuplai oleh perusahaan farmasi di China dan India. Para ahli memperkirakan dua pertiga bahan obat aktif datang dari dua negara tersebut."Kami harus mulai berpikir secara global dan bekerja strategis dengan para rekan di seluruh dunia bagaimana caranya memaksimalkan kapasitas pengawasan kita. Jadi pasien bisa yakin dengan kualitas, keamanan, dan efikasi semua obat di manapun diproduksi," komentar Direktur Eksekutif Badan Pengawas Obat Eropa Guido Rasi terhadap kasus ini.
Menurut keterangan BPOM valsartan adalah obat oral yang masuk dalam kategori antagonis reseptor angiotensin II. Obat dalam kategori tersebut bekerja dengan cara menghambat reseptor angiotensin yang dapat berujung pada pelebaran pembuluh darah.
Ketika pembuluh darah melebar maka tekanan darah akan berkurang.
Karena sifatnya yang dapat melebarkan pembuluh darah valsartan sering dipakai untuk mengobati hipertensi dan gagal jantung. Kadang valsartan juga dipakai pada kasus serangan jantung untuk mengurangi risiko kematian dan waktu perawatan di rumah sakit.
Valsartan awalnya dikembangkan oleh perusahaan farmasi Norvatis asal Swiss dengan nama Diovan. Tapi setelah patennya habis di tahun 2012 banyak perusahaan menggunakannya untuk membuat obat generik termasuk oleh Zhejiang Huahai.
Obat mengandung valsartan yang diproduksi Zhejiang Huahai ditarik karena ditemukannya zat pengotor NDMA. Menurut ahli kemungkinan ini terjadi ketika perusahaan mengubah proses produksinya di tahun 2012.
NDMA dalam beberapa studi disebut berhubungan dengan risiko kanker. Para ahli di Badan Pengawas Obat Eropa mengaku masih mengukur dampak pada pasien akibat konsumsi obat valsartan yang terkontaminasi ini.
Menurut Reuters saat ini kebutuhan obat valsartan di seluruh dunia banyak disuplai oleh perusahaan farmasi di China dan India. Para ahli memperkirakan dua pertiga bahan obat aktif datang dari dua negara tersebut.
"Kami harus mulai berpikir secara global dan bekerja strategis dengan para rekan di seluruh dunia bagaimana caranya memaksimalkan kapasitas pengawasan kita. Jadi pasien bisa yakin dengan kualitas, keamanan, dan efikasi semua obat di manapun diproduksi," komentar Direktur Eksekutif Badan Pengawas Obat Eropa Guido Rasi terhadap kasus ini.
























































